近日中国科学技术大学翁建平、刘连新教授团队在Science Bulletin发表了题为“Hepatic IFRD1 suppresses metabolic dysfunction-associated fatty liver disease via GLUD1/α-KG axis”的论文,[1] 首次揭示了干扰素相关发育调节因子1(IFRD1)通过调控谷氨酸脱氢酶1(GLUD1)介导的α-酮戊二酸(α-KG)生成,形成代谢-表观遗传调控轴抑制肝脏从头脂肪生成(DNL)的分子机制,为代谢功能障碍相关脂肪性肝病(MASLD)的精准治疗提供了全新靶点与策略。
MASLD已成为全球发病率最高的慢性肝病,可从单纯性肝脂肪变逐步进展为MASH、肝硬化,甚至肝细胞癌,严重威胁人类健康。[2] 然而,目前仅有两款药物获美国FDA批准用于MASLD治疗,临床亟需开发新的有效治疗手段。[3] 肝脏从头脂肪生成(DNL)异常激活是MASLD核心病理特征,[4] 靶向DNL通路已成为该领域药物研发的关键方向,但现有靶点仍难以满足临床需求,探索新的调控机制迫在眉睫。
该研究通过临床样本分析与多种小鼠模型验证,取得了系列创新性发现:
一、临床关联与动物实验验证:明确IFRD1在MASLD中的保护作用
研究团队首先在人肝组织中证实,IFRD1的表达水平与MASLD疾病进展呈显著负相关。在动物模型中,Ifrd1敲除小鼠的MASLD病理表型显著加重;而肝细胞特异性过表达Ifrd1则能有效抑制疾病进展,明确了IFRD1在MASLD中的保护作用及靶向潜力。
二、解析分子调控新机制,搭建代谢—表观遗传桥梁
机制研究揭示,IFRD1通过结合GLUD1的N端1-70位氨基酸,发挥双重调控作用:一方面促进GLUD1的线粒体定位,另一方面稳定其酶活性,最终显著增强α-KG的生成。作为三羧酸循环的核心中间代谢产物,α-KG进一步通过表观遗传调控发挥作用——降低脂肪生成相关基因启动子区域的H3K36me3修饰富集,直接抑制肝脏从头脂肪生成过程,从而改善MASLD病理进程。
三、验证干预策略可行性,揭示发现的转化潜力
尤为重要的是,外源性补充α-KG可有效逆转肝脏条件性Ifrd1敲除小鼠的MASLD加重表型,这一发现证实了α-KG在疾病干预中的关键作用,为开发基于代谢中间体的治疗策略提供了坚实的实验依据。
对临床样本进行再次分析显示,MASLD患者肝脏中GDH酶活性和α-KG含量均显著降低,H3K36me3水平升高,且与IFRD1表达呈相关性,证实该调控轴在人类MASLD发病机制中同样发挥关键作用。
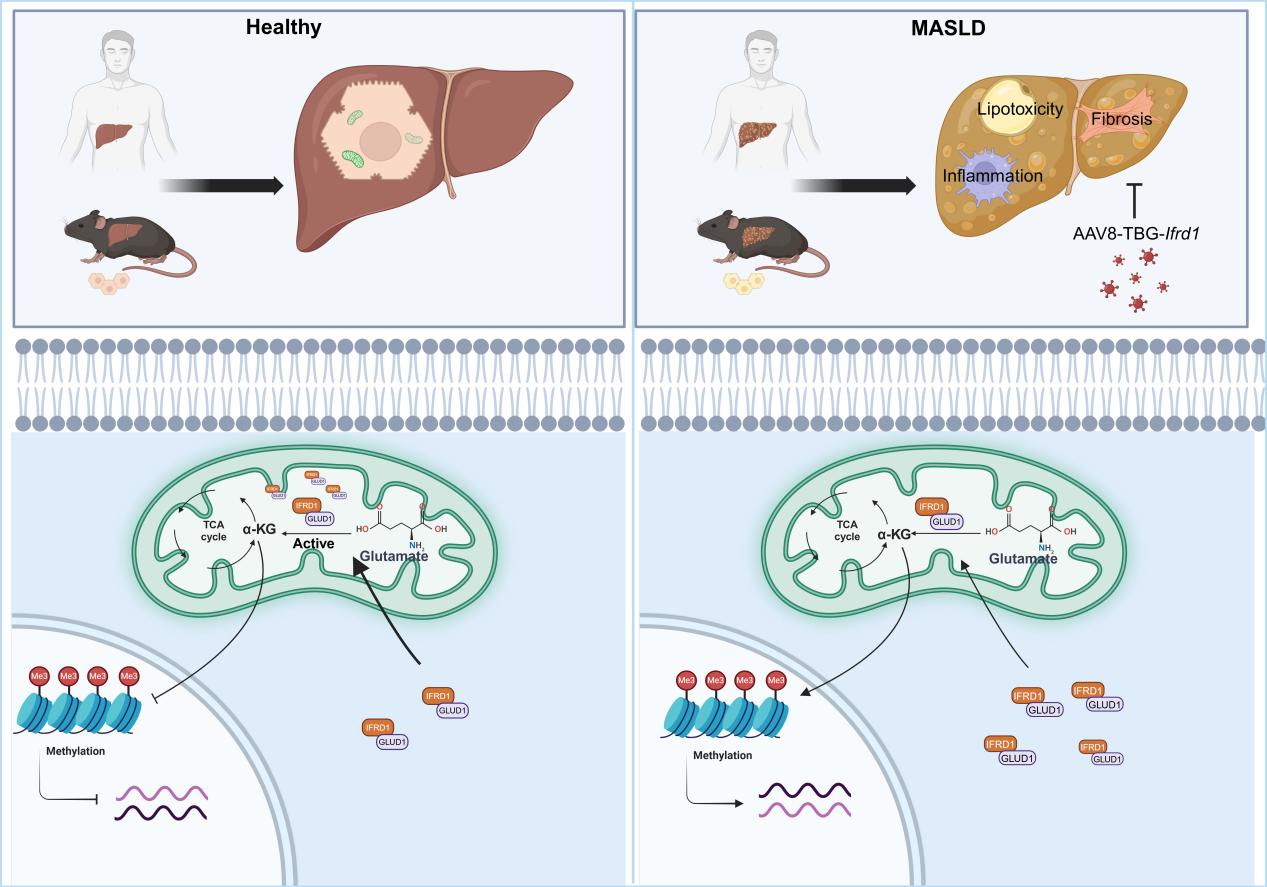
该研究系统阐明了IFRD1-GLUD1-α-KG轴作为连接代谢调控与表观遗传修饰的关键通路,其创新价值体现在三个方面:一是首次建立了IFRD1与MASLD进展的临床关联,明确其作为疾病保护因子的功能;二是揭示了GLUD1酶活性参与调控MASLD的新机制;三是验证了代谢中间体α-KG的表观遗传调控作用,为MASLD的“代谢—表观遗传”靶向治疗提供了新范式。
参考文献:
[1] Science Bulletin. 2026 Apr: Online ahead of print.DOI:10.1016/j.scib.2026.04.016
[2] Lancet Reg Health Eur. 2025 Jun 4:54:101320. doi:10.1016/j.lanepe.2025.101320.
[3] Lancet Gastroenterol Hepatol. 2026 Feb 13:S2468-1253(25)00323-1.doi:10.1016/S2468-1253(25)00323-1.
[4] Gastroenterology.2014 Mar;146(3):726-35.·doi:10.1053/j.gastro.2013.11.049.
